חנקן חמצני
| חנקן חמצני | ||
|---|---|---|
 | ||
 | ||
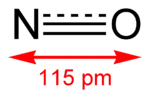
| מולקולת חנקן חמצני | ||
| נוסחה כימית | NO | |
| מסה מולרית | 30.0061±0.0005 | |
| מראה | חסר צבע | |
| מספר CAS | 10102-43-9 | |
| מצב צבירה | גז | |
| טמפרטורת היתוך | -163.6 | |
| טמפרטורת רתיחה | -151.8 | |
| בליעה אופטית | 1.0002697 | |
התרכובת חנקן חמצני (או חנקן חד-חמצני) היא מולקולה המורכבת מאטום אחד של חמצן ואטום אחד של חנקן שסימולו NO. בתנאים סטנדרטיים של טמפרטורה ולחץ תרכובת זו היא גז. זהו מוליך עצבי חשוב בגופם של יונקים, כולל האדם, ומולקולת האיתות היחידה שהיא גז.
אין לבלבל בין מולקולה זו לחמצן דו-חנקני שהוא חומר הרדמה וגז חממה או לחנקן דו-חמצני שהוא גז רעיל מאד בצבע חום ואחד ממזהמי האוויר העיקריים (נפלט ממנוע בעירה פנימית). אולם, חנקן חמצני מתחמצן מהר מאד באוויר והופך לחנקן דו-חמצני ניתן להבחין בתהליך זה בהופעתו של צבע אדמדם-חום.
מולקולות חנקן חמצני היא רדיקל חופשי, ולכן הראקטיביות גבוהה. זמן מחצית החיים שלו הוא בין שנייה לחמש שניות[1].
תגובות כימיות נפוצות
- כאשר שתי מולקולות של חנקן חמצני נפגשות עם מולקולת חמצן, נוצר חמצון לשתי מולקולות של חנקן דו-חמצני:
- 2 NO + O2 → 2 NO2
- כאשר החמצון קורה במים אז מולקולת מים, חמצן וחנקן חמצני יוצרים חומצה חנקיתית:
- 4 NO + O2 + 2 H2O → 4 HNO2
ייצור
על מנת ליצור חנקן חמצני משתמשים בתהליכים כימיים בחום גבוה.
- בתהליך אוסטוולד התעשייתי משתמשים בחמצון אמוניה בטמפרטורה שבין 750 °C לבין 900 °C (בדרך כלל 850 °C) כאשר סגסוגת פלטינה - רודיום משמש כזרז:
- 4 NH3 + 5 O2 → 4 NO + 6 H2O
- דרך אחרת ליצור זאת הוא בשימוש במולקולות חמצן וחנקן פשוטות בטמפרטורה גבוהה מאד (מעל 2000 °C). תהליך זה אינו פרקטי ולא נמצא בשימוש:
- N2 + O2 → 2 NO
- במעבדות משתמשים בחנקות ובחומצה חנקתית. למשל בשימוש בנחושת חנקיתי:
- 8 HNO3 + 3 Cu → 3 Cu(NO3)2 + 4 H2O + 2 NO
- תהליך דומה בשימוש בנתרן חנקיתי או באשלגן חנקיתי:
- 2 NaNO2 + 2 NaI + 2 H2SO4 → I2 + 4 NaHSO4 + 2 NO
- 2 NaNO2 + 2 FeSO4 + 3 H2SO4 → Fe2(SO4)3 + 2 NaHSO4 + 2 H2O + 2 NO
- 3 KNO2 (l) + KNO3 (l) + Cr2O3(s) → 2 K2CrO4(s) + 4 NO
ראו גם
הערות שוליים
- ↑ Gabbai, F. B., Garcia, G. E. et al., Role of nitric oxide in glomerular physiology and pathophysiology, Adv Nephrol Necker Hosp 24, 3-18 (1995)
This article is issued from Hamichlol. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.